1 / 1
Processus De Synthèse D'intermédiaire D'Omarigliptine CAS 951127-25-6
| Model No. : | 951127-25-6 |
|---|---|
| Brand Name : | VOLSENCHEM |
Taizhou, Zhejiang, China
- Fabricant
- Service OEM
- Fournisseur or

- Certification de plate-forme

- Expo en ligne

Description du produit
Omarigliptine intermédiaire numéro CAS 951127-25-6, également connu comme intermédiaire CPo3604-01, formule moléculaire: C16H19F2NO4, poids moléculaire: 327.32, son procédé de synthèse est le suivant:
31,2 g de NaOH ont été dissous dans un mélange d'eau et de méthanol, le réfrigérant à base d'éthanol a été refroidi à 0 ° C et, au bout de 30 minutes, 57,3 ml de 2,5-difluorobenzaldéhyde et 42,6 ml de nitrométhane ont été ajoutés goutte à goutte. Après la réaction, le mélange a été neutralisé avec de l'acide acétique, agité avec de l'acétate d'éthyle et la couche organique a été lavée successivement avec une solution de carbonate de sodium et de la saumure, séchée sur du sulfate de sodium anhydre, filtrée et concentrée pour donner le 2-nitro-1. 5- 112 g de difluorophényl) -éthanol, désigné ci-après intermédiaire I.
100 g d'intermédiaire I ont été dissous dans 200 ml d'acétone et refroidis à 0 ° C, 90 g de réactif de Jones ont été ajoutés goutte à goutte, la température de la solution réactionnelle a été maintenue à 3 ° C, une fois la réaction terminée, la solution réactionnelle a été refroidie à moins de 0 ° C. On a ajouté goutte à goutte du et 50 ml d'isopropanol pour détruire l'excès. Le réactif de Jones, filtré et lavé à l'acétone, le filtrat et le liquide de lavage ont été combinés, évaporés à sec pour donner un liquide huileux vert clair, qui a été refroidi dans un bain de glace et 1 L d'eau froide a été ajouté pour précipiter un solide blanc. qui a été filtré et lavé à l'eau et séché pour donner le 2-nitro-1 (2), 5-difluorophényl) -acétaldéhyde 62,3 g, appelé ci-après l'intermédiaire II.
50,85 ml de 1,3-dichloro-2-propanol et 54,7 g de l'intermédiaire II ont été dissous dans du DMF, et 176 g de Cs2CO3 y ont été ajoutés et mis à réagir à 25 à 30 pendant 4 heures, et le liquide réactionnel a été filtré et le résidu a été lavé avec de l'éther diisopropylique. Le filtrat a été versé dans 1,75 L / 1 N d'acide chlorhydrique froid et extrait deux fois avec 850 ml d'éther isopropylique. L'extrait a été lavé avec de la saumure saturée et les couches ont été séparées. Le solvant a été évaporé à sec. Le mélange a été lavé et séché pour donner 37,1 g de 2- (2,5-difluorophényl) -3-nitro-5-hydroxytétrahydro-pyrane, ci-après désigné l'intermédiaire III.
35,6 g de l'intermédiaire III ont été dissous dans 125 ml de méthanol, 16 g de NaBH4 ont été ajoutés par lots en l'espace de 30 min, la température a été contrôlée à 0-5 ° C et le mélange a été agité à 0-5 ° C pendant 30 min après l'addition. puis 0,5 L / 6 N d'HCl a été ajouté goutte à goutte pour terminer la réaction. 1,05 L d'eau glacée, agitée à 0 ° C et précipitée sous forme d'un solide blanc, filtrée, lavée à l'eau et séchée pour donner le 2- (2,5-difluorophényl) -3-nitro-5-hydroxytétrahydro-pyranose.Le solide obtenu ci-dessus a été ajouté à 92 ml d'isopropanol, chauffé à 92 ° C pour se dissoudre, puis lentement refroidi pour précipiter le trans-2- (2,5-difluorophényl) -3-nitro-5-hydroxytétrahydro-Pyran, filtré, lavé à l'isopropanol, séché donner un produit trans de 16,9 g. Le filtrat a été concentré à sec. Le résidu a été combiné avec du THF. Le solvant a été évaporé pour donner le diastéréoisomère (13,4 g). Le traitement à l'isopropanol par le procédé décrit ci-dessus a donné 7,4 g de trans-2- (2,5-difluorophényl) -3-nitro-5-hydroxytétrahydropyrane. On ajoute 100 ml d’isopropanol à 24,3 g de trans-2- (2,5-difluorophényl) -3-nitro-5-hydroxytétrahydropyrane obtenu aux deux étapes ci-dessus, on chauffe à 90 ° C pour le dissoudre, puis on refroidit à à température ambiante, cristallisée, filtrée, lavée avec de l'alcool isopropylique et séchée pour donner 21,5 g de trans-2- (2,5-difluorophényl) -3-nitro-5-hydroxytétrahydropyrane, ci-dessous désigné sous le nom d'intermédiaire IV.
20,7 g de l'intermédiaire IV ont été dissous dans 100 ml de méthanol, ajoutés à un récipient réactionnel à haute pression, 3 g de catalyseur de Raney Ni ont été ajoutés, l'hydrogène a été remplacé, la pression d'H 2 était de 2,5 MPa, 40 et la réaction a été filtrée. 3 h et le filtrat a été désolvaté pour obtenir le trans-2. - (2,5-difluorophényl) -3-amino-5-hydroxytétrahydro-2H-pyranne brut, 18,7 g, appelé ci-après intermédiaire V.
10,5 g d'acide D (-) tartrique ont été dissous dans 100 ml de méthanol et un mélange de 17 g d'intermédiaire V et 59,5 ml de méthanol y a été ajouté, agité à 25 pendant 15 h, filtré, lavé avec du méthanol et séché et le solide obtenu a été chauffé au reflux dans 119 ml de méthanol. 1 h, refroidir lentement à température ambiante et agiter pendant 15 h. Le solide a été filtré à nouveau, lavé avec du méthanol et séché pour donner 14,2 g de tarte. Le sel d'acide tartrique obtenu a été dissous dans 200 ml d'un solvant mixte d'acétonitrile et d'eau, 10 g de Na2CÛ3 ont été ajoutés par portions à 25-30 ° C, la solution réactionnelle a été refroidie à 0-5 ° C et 15,3 g de BOC ajouté plus loin. Après agitation pendant 2 heures, l'acétonitrile a été éliminé par distillation et la solution résiduelle a été distillée. On a ajouté 150 ml d'eau glacée et agité pendant 30 minutes, puis le solide a été filtré, lavé à l'eau et séché pour donner un solide blanc (2R, 3S) -2- (2,5-difluorophényl) -5-hydroxytétrahydro-2H. -pyrane 11,7 g d’acide 3-carbamique de tert-butyle, appelé ci-après intermédiaire VI.
10 g de l'intermédiaire VI ont été dissous dans 50 ml de dichlorométhane et 6 g de CrO3 y ont été ajoutés, et le mélange a été agité à température ambiante pendant 3 heures, laissé au repos et les couches ont été séparées. Les phases organiques ont été combinées et lavées avec du Na2S2O3 à 10%, de l'eau et de la saumure. La phase organique a été séchée sur du sulfate de sodium anhydre et évaporée à sec pour donner un intermédiaire à l'omarigliptine.
Spécifications de qualité de l'ester 1,1-di-méthyléthylique de l'acide N - [(2R, 3S) -2- (2,5-difluorophényl) tétrahydro-5-oxo-2H-pyran-3-yl] -CarbaMique CAS 951127-25 -6 est l'impureté totale ≤1,0%, l'impureté simple ≤0,50%, la perte au séchage ≤0,50%.
Thera. Catégorie : Anti Diabetes
Numéro de cas : 951127-25-6
Synonyme : CPo3604-01; [(2R, 3S) -5-oxo-2- (2,5-difluorophényl) tétradihydro-2H-pyran-3-yl] carbamate de tert-butyle [(2R, 3S)] Le (2- (2,5-difluorophényl) -5-oxotétrahydro-2H-pvran-3-yl] carbamate de tert-butyle ((2R, 3S) -2- (2,5-difluorophényl) -5-oxotétrahydro-2H- pyran-3-yl) carbamate; ester 1,1-di-méthyléthylique de l'acide N - [(2R, 3S) -2- (2,5-difluorophényl) tétrahydro-5-oxo-2H-pyran-3-yl] -CarbaMique; Produit NaMe: MK-3102 intermédiaire; Omarigliptine inter.
Formule moléculaire : C16H19F2NO4
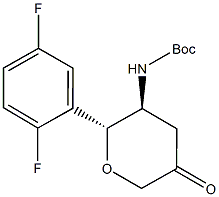
Poids moléculaire: 327.32
Dosage: ≥98.%
Apparence: solide cristallin blanc
Stockage : normal
Emballage : emballage digne d'exportation
Fiche de données de sécurité : disponible sur demande
Intermédiaire connexe:
1) Ester 1,11-di-méthyléthylique de l'acide N - [(2R, 3S) -2- (2,5-difluorophényl) tétrahydro-5-oxo-2H-pyran-3-yl] -Carbamique 951127-25-6
2) le 2- (méthylsulfonyl) -2,4,5,6-tétrahydropyrrolo [3,4-c] pyrazole, CAS 1280210-80-1,
Taizhou, Zhejiang, China
- Fabricant
- Service OEM
- Fournisseur or

- Certification de plate-forme

- Expo en ligne
Envoyez votre demande à ce fournisseur






![(1R,5S)-3-ethyl-Bicyclo[3.2.0]hept-3-en-6-one Used For Mirogabalin Cas 1235479-61-4](http://bsg-i.nbxc.com/product/ce/32/94/8ba8889bfb970f2a0aec2e61ea.gif?x-oss-process=image/resize,w_220,h_220)


![2-(Methylsulfonyl)-2,4,5,6-tetrahydropyrrolo[3,4-c]pyrazole For Omarigliptin 1280210-80-1](http://bsg-i.nbxc.com/product/fe/ee/4f/75922bff8435f27122f16c966e.gif?x-oss-process=image/resize,w_220,h_220)


![Benzene,4-bromo-1-chloro-2-[(4-ethoxyphenyl)methyl]- For Making Sotagliflozin CAS 461432-23-5](http://bsg-i.nbxc.com/product/fb/e0/e4/79a02f2374591b03964ae309f8.gif?x-oss-process=image/resize,w_220,h_220)




![1,2,6,7-tétrahydro-8H-Indeno [5,4-b] Furan-8-One CAS 196597-78-1](http://bsg-i.nbxc.com/product/4c/63/e8/8acd1e9ac80369a5298ffee447.jpg?x-oss-process=image/resize,w_220,h_220)







![Carbamate de (5-tosyl-5H-pyrrolo [2,3-B] pyrazine-2-yl) de tert-butyle pour l'upadacitinib CAS 1201187-44-1](http://bsg-i.nbxc.com/product/f6/53/59/a3789b2d2e70c69d7aa41eacf4.jpg?x-oss-process=image/resize,w_220,h_220)
![(3S, 4R) -3-éthyl-4- (3H-imidazo [1,2-a] pyrrolo [2,3-e] pyrazin-8-yl) pyrrolidine-1-carboxylate de benzyle 2095311-51-4](http://bsg-i.nbxc.com/product/81/f2/52/a11669ef7481d367c2a0a8d9d6.gif?x-oss-process=image/resize,w_220,h_220)
